
Abstrak Grafis
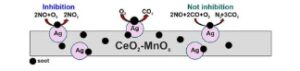
Ag/CeO 2 , Ag/MnO x , dan Ag/CeMnO x (pada rasio molar Ce/Mn yang berbeda) yang disintesis melalui metode sol-gel sitrat diteliti dalam oksidasi jelaga. Keberadaan NO dalam campuran reaksi menghambat oksidasi jelaga. Dengan menambahkan CO ke dalam campuran reaksi NO + O 2 tidak diamati adanya penghambatan pembakaran jelaga, dan NO diubah menjadi N 2 melalui SCR dengan CO sebelum oksidasi totalnya menjadi CO 2 .
Abstrak
Studi ini menyelidiki efektivitas dalam oksidasi jelaga di bawah kontak rapat dan longgar katalis Ag/CeO2 , Ag/MnOx , dan Ag/CeMnOx dengan rasio molar Ce:Mn yang berbeda yang disiapkan dengan metode sol-gel sitrat. Metode sol-gel mendorong pembentukan struktur nanodomain dalam komposit CeMnOx . Interaksi antara oksida serium dan mangan dan rasio Ce/Mn adalah faktor kunci untuk membentuk struktur nanodomain tersebut. Rasio Ce/Mn 1:1 memberikan aktivitas dan stabilitas tinggi dengan mencegah sintering nanopartikel CeO2 , sementara pada rasio Ce/Mn yang berbeda, penonaktifan akhirnya terjadi. Kehadiran NO dalam campuran reaksi menghambat oksidasi jelaga, sementara keberadaan CO dalam campuran NO + O2 membatasi efek tersebut. Katalis Ag/ CeMnOx yang paling menjanjikan dengan rasio Ce/Mn 1:1 berhasil diaplikasikan pada monolit kordierit. Baik katalis bubuk maupun monolitik secara selektif mengoksidasi jelaga menjadi CO2 masing -masing di bawah 500 dan 600 °C, yang menunjukkan hal ini menjanjikan untuk aplikasi praktis dalam oksidasi jelaga yang efisien.
1 Pendahuluan
Mesin diesel yang dikenal karena performa tenaga yang kuat dan efisiensi bahan bakar yang tinggi dianggap sebagai sumber tenaga yang menjanjikan untuk kendaraan ringan, yang sebagian besar mengandalkan mesin bensin. Namun, adopsi mesin diesel secara luas terhambat oleh masalah emisi yang signifikan, khususnya pelepasan partikel (PM) yang sebagian besar terdiri dari jelaga. Jelaga terdiri dari campuran kompleks partikel karbon dan senyawa organik dan terutama dihasilkan karena pembakaran bahan bakar hidrokarbon yang tidak sempurna. [ 1 ] Polutan ini memiliki risiko lingkungan dan kesehatan yang serius. [ 2 ]
Di antara semua solusi, salah satu yang layak dan sangat efektif adalah penggunaan filter katalitik, khususnya filter partikulat diesel (DPF), yang memerangkap dan mengoksidasi jelaga secara efektif sehingga mengurangi dampak buruknya dengan menurunkan suhu oksidasi jelaga secara signifikan. [ 3 , 4 ] Dengan menggabungkan katalis, DPF dapat menurunkan suhu oksidasi jelaga dari 600 °C yang biasa ke rentang operasi yang lebih praktis, biasanya sekitar 250–400 °C, sehingga membuatnya efektif pada suhu gas buang diesel yang umum (175–400 °C). Oksidasi yang dikatalisis ini memungkinkan regenerasi jelaga secara terus-menerus yang mencegah penyumbatan filter dan mempertahankan kinerja mesin yang optimal. [ 4 ]
Banyak pekerjaan eksploratif dan perintis telah dilakukan untuk mengembangkan katalis yang efisien untuk reaksi ini, termasuk oksida logam tunggal dan campuran serta katalis berbasis logam mulia. [ 1 , 5 – 9 ] Di antara ini, cerium oksida (CeO₂) sangat dihargai karena aktivitas katalitiknya yang luar biasa, khususnya untuk perilaku redoks antara Ce⁴⁺ dan Ce 3 ⁺ dalam kondisi oksidasi dan reduksi. [ 5 , 9 – 11 ] Kapasitas penyimpanan oksigennya yang unik memungkinkan material untuk menyimpan dan melepaskan spesies oksigen yang sangat aktif. [ 10 , 11 ] Demikian pula, mangan oksida (MnO x ) banyak digunakan dalam reaksi oksidasi dan reduksi, yang terkait dengan keadaan oksidasi multivalennya (terutama Mn 2 ⁺, Mn 3 ⁺, dan Mn⁴⁺) dan mobilitas oksigen kisi yang tinggi. [ 1 , 8 , 12 ]
Bahasa Indonesia: Bila dikombinasikan, katalis MnO x -CeO₂ menunjukkan aktivitas katalitik yang unggul yang secara signifikan menurunkan suhu penyalaan untuk oksidasi jelaga karena efek sinergis antara dua oksida logam. [ 13 – 15 ] Penggabungan mangan ke dalam kisi ceria meningkatkan mobilitas oksigen aktif yang memfasilitasi evolusi oksigen kisi, yang mendukung oksidasi jelaga. [ 14 – 16 ] Selain itu, kekosongan oksigen yang terbentuk ketika oksigen aktif tumpah dari katalis ke permukaan jelaga memainkan peran penting dalam proses ini karena kemudian diisi oleh gas O₂ yang mengoksidasi ulang katalis. [ 16 , 17 ] Penambahan perak (Ag) ke katalis CeO₂ dan MnO x juga secara signifikan meningkatkan reaktivitasnya untuk oksidasi jelaga. [ 9 , 18 , 19 ] Faktanya, nanopartikel Ag meningkatkan kinerja katalitik secara keseluruhan dengan memfasilitasi pembentukan spesies oksigen reaktif dan meningkatkan kontak antara katalis dan partikel jelaga. Sinergi ini mempercepat proses oksidasi dan berkontribusi untuk menurunkan energi aktivasi yang diperlukan untuk pembakaran jelaga. [ 19 , 20 ] Dengan demikian, katalis CeO₂-MnO x yang dimodifikasi Ag untuk aplikasi suhu rendah dianggap menjanjikan untuk pengurangan jelaga yang efektif.
Namun, sebagian besar penelitian menunjukkan aktivitas sampel yang baru disiapkan, [ 13 , 14 , 16 – 21 ] sementara stabilitas termal sistem tersebut masih menjadi masalah untuk penggunaannya. [ 1 , 8 , 12 , 15 , 22 ] Beberapa pendekatan diusulkan untuk meningkatkan stabilitas termal katalis CeO₂-MnO x , seperti penambahan Al 2 O 3 15 atau Y 2 O 3 , [ 22 ] yang mencegah sintering oksida mangan dan ceria, penggunaan nanomaterial 1D, 2D, [ 1 ] dan seterusnya. Selain itu, hasil aktivitas katalis biasanya diperoleh dengan menggunakan sampel bubuk yang dicampur dengan jelaga dan secara signifikan bergantung pada banyak faktor termasuk jenis jelaga model, dispersi komponen, derajat homogenisasi campuran, komposisi granulometri bubuk, rasio antara komponen campuran, dan kepadatan pemadatan. [ 5 , 6 ] Pada kasus campuran jelaga-katalis, kondisi kontak longgar masih jauh dari kondisi operasi filter jelaga, sedangkan penelitian pada katalis monolit masih jarang.
Tujuan dari penelitian ini adalah untuk mengevaluasi kinerja katalis Ag/CeMnO x dalam pembakaran jelaga di bawah kontak rapat menggunakan sampel bubuk dan di bawah kondisi kontak longgar menggunakan sampel monolit di bawah aliran O 2 /He serta di hadapan NO dan NO─CO. Sistem katalitik ini dinilai efektivitasnya dalam oksidasi jelaga melalui spesies “oksigen aktif”. Penelitian ini difokuskan pada pemahaman peran formulasi katalis ini dalam meningkatkan oksidasi jelaga dan stabilitas termal yang menyoroti potensinya untuk memfasilitasi mekanisme yang digerakkan oleh oksigen aktif.
2 Hasil dan Pembahasan
2.1 Struktur dan Aktivitas Oksidasi Jelaga Katalis Serbuk
Serangkaian katalis bubuk yaitu, Ag/CeO2 ( disebut sebagai Ag/Ce), Ag/MnOx ( disebut sebagai Ag/Mn), dan Ag/CeMnOx dengan rasio molar Ce:Mn yang berbeda (3:1, 1:1, dan 1:3; masing-masing disebut sebagai Ag/3Ce1Mn, Ag/1Ce1Mn, dan Ag/1Ce3Mn) dengan kandungan Ag nominal 1 wt.% dipelajari dalam oksidasi jelaga menggunakan kondisi kontak ketat untuk menentukan komposisi katalis terbaik dalam hal aktivitas dan stabilitas. Pendukung oksida disiapkan dengan metode sol-gel sitrat, sementara Ag dimasukkan melalui impregnasi kebasahan awal dari larutan berair [Ag(NH3 ) 2 ] NO3 ( untuk rincian lihat Informasi Pendukung (SI)).
Data XRD (Tabel 1 , Gambar S1 ) menunjukkan keberadaan fase tipe fluorit terdispersi dengan parameter kisi a = 5,405–5,413 Å yang sesuai dengan CeO 2-δ tak terdoping dalam semua sampel yang mengandung Ce. Beberapa peningkatan dalam parameter kisi fase fluorit untuk sampel Ag/CeMnO x dapat dikaitkan dengan peningkatan kandungan ion Ce 3+ (jari-jari ionik (ir) sebesar 1,28 Å dibandingkan dengan 0,97 Å untuk ion Сe 4+ ) daripada penggabungan ion Mn 4+ atau Mn 3+ yang lebih kecil (ir masing-masing sebesar 0,79 dan 0,67 Å). Fase Mn2O3 dan Mn3O4 individual juga terungkap untuk sampel Ag/1Ce3Mn dengan kandungan Mn tinggi mirip dengan katalis Ag/Mn (Tabel 1 , Gambar S1 ), dengan spektrum Raman yang mengonfirmasi keberadaan fase MnOx dalam semua sampel Ag/CeMnOx ( Gambar S2 ). Tidak ada sinyal yang dikaitkan dengan spesies Ag2O / Ag yang diidentifikasi dalam sampel melalui XRD, yang menunjukkan dispersi perak yang tinggi.
Tabel 1. Adsorpsi nitrogen suhu rendah (luas permukaan spesifik (SSA)) dan data XRD (grup ruang (SG), parameter kisi ( a, c ), dan ukuran kristalit rata-rata ( D XRD ) untuk fase yang diamati) untuk sampel awal dan lama.
Data HR TEM dengan analisis HR EDX mengungkap mikrostruktur domain untuk sampel Ag/CeMnO x (Gambar 1 ) yang dibentuk oleh nanokristalit yang diperkaya oleh Mn atau Ce. Metode sol-gel sitrat menghasilkan pembentukan komposit CeMnO x dengan mikrostruktur nanodomain karena pencampuran komponen yang seragam selama pembentukan gel dan kelarutan MnO x yang terbatas dalam struktur fluorit CeO2. [ 23 ] Distribusi kristalit yang berbeda dalam mikrostruktur domain bergantung pada rasio Ce:Mn dan paling acak untuk sampel Ag/1Ce1Mn, sementara untuk sampel lain terjadi penggumpalan kristalit dengan jenis yang sama (untuk komponen yang berlebih). Menurut analisis HR EDX, perak terdistribusi secara seragam di atas sampel dengan pembentukan ion Ag + di permukaan atau di daerah bawah permukaan matriks pendukung oksida yang sebelumnya ditunjukkan oleh XPS. [ 24 ]

Gambar 1
Buka di penampil gambar
Presentasi PowerPoint
Gambar HR STEM dan pemetaan HR EDX khas untuk material Ag/CeMnO x yang dicontohkan oleh sampel Ag/1Ce1Mn.
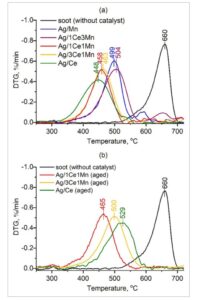
Gambar 2a menunjukkan hasil studi aktivitas katalitik dalam kondisi kontak rapat. Dengan adanya katalis, suhu pembakaran jelaga menurun secara signifikan terhadap proses tanpa katalis dan jelaga teroksidasi sepenuhnya menjadi CO 2 , sementara tanpa katalis apa pun, baik CO maupun CO 2 terbentuk (Gambar S3 ). Sampel Ag/Mn dan Ag/1Ce3Mn menunjukkan aktivitas terendah (~50% konversi jelaga dicapai pada ~500 °C). Peningkatan lebih lanjut dalam kandungan Ce dalam matriks oksida menghasilkan peningkatan aktivitas katalis, dengan sampel Ag/Ce menunjukkan aktivitas tertinggi ( T maks = 448 °C). Ini menyoroti peran penting ceria yang terdispersi dalam komposit Ag/CeMnO x dalam pembakaran jelaga.
Gambar 2
Buka di penampil gambar
Presentasi PowerPoint
Ketergantungan suhu terhadap laju oksidasi jelaga untuk katalis bubuk segar dan katalis yang disimpan pada suhu 650 °C selama 12 jam.
Penuaan termal pada 650 °C selama 12 jam menyebabkan penonaktifan signifikan Ag/Ce (yang sudah tua) ( T maks = 529 °C, ΔT maks = 81°) karena peningkatan signifikan ukuran kristalit dari 15 menjadi 43 mn dan penurunan kuat SSA dari 34 menjadi 14 m 2 /g (Tabel 1 ). T maks pembakaran jelaga pada Ag/3Ce1Mn (yang sudah tua) juga meningkat hingga 500 °C ( ΔT maks = 37 °C) karena sintering sampel (Tabel 1 ). Hasil ini konsisten dengan yang dilaporkan oleh Wu untuk CeO 2 dan MnO x -CeO 2 dengan rasio molar Mn/Ce sebesar 15:85. [ 14 , 15 ] Sebaliknya, Ag/1Ce1Mn (yang sudah tua) tampak paling stabil dengan kinerja oksidasi tertinggi ( T maks = 465 °C, ΔT maks = 7°) (Gambar 2b ). Hal ini terkait dengan pembentukan mikrostruktur nanodomain stabil yang dibentuk oleh nanokristalin CeO 2 dan MnO x yang terdistribusi secara acak untuk penyangga komposit CeMnO x yang mencegah sintering Ag/1Ce1Mn yang kuat dan memastikan aktivitas dan stabilitasnya yang tinggi dalam oksidasi jelaga yang berbeda dengan sampel Ag/Ce dan Ag/3Ce1Mn yang dinonaktifkan setelah penuaan. Dengan demikian, ukuran kristalit katalis, Ag/1Ce1Mn, meningkat hingga 12 nm dan SSA menurun hingga 21 m 2 /g. Sebelumnya telah ditunjukkan bahwa Ag/1Ce1Mn menunjukkan aktivitas dan stabilitas tinggi dalam reduksi katalitik selektif (SCR) NO. 24
2.2 Oksidasi Jelaga dalam Kehadiran NO x dan NO x ─CO
Oksidasi jelaga dengan adanya NO x dan NO x ─CO dalam gas umpan juga dipelajari untuk sampel bubuk Ag/1Ce1Mn dalam kondisi kontak rapat dalam reaktor aliran tubular menggunakan mode reaksi terprogram suhu (TPR) dan penganalisa gas untuk mendeteksi CO, CO 2 , O 2 dalam aliran reaksi (untuk rincian lihat SI). Gambar 3 menunjukkan profil konsentrasi CO 2 dan CO selama oksidasi jelaga pada sampel Ag/1Ce1Mn dalam aliran 10 vol.% O 2 dalam helium, 10 vol.% O 2 , 0,1 vol.% NO dalam helium, dan 10 vol.% O 2 , 0,1 vol.% NO, 1,25 vol.% CO dalam helium.
Gambar 3
Buka di penampil gambar
Presentasi PowerPoint
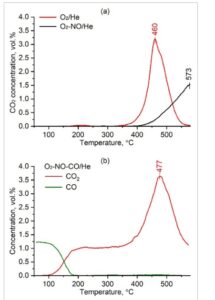
Profil CO2 dan konsentrasi CO selama oksidasi jelaga pada sampel Ag/1Ce1Mn dengan campuran reaksi yang berbeda: (a) 10 vol.% O2 dalam helium dan 10 vol.% O2 , 0,1 vol.% NO dalam helium ; (b) 10 vol.% O2 , 0,1 vol.% NO, 1,25 vol.% CO dalam helium; laju aliran gas adalah 40 ml/menit pada kedua kasus.
Menurut hasil yang diperoleh (Gambar 3a ), oksidasi jelaga pada katalis Ag/1Ce1Mn dalam aliran 10 vol.% O 2 dalam helium pada mode TPR dalam reaktor tubular terjadi pada kisaran 320–550 °C dengan laju oksidasi maksimum pada 460 °C untuk membentuk hanya CO 2 sebagai produk (Gambar 2a ). Penambahan NO ke dalam campuran reaksi menghambat proses pembakaran jelaga. Dalam kasus ini, oksidasi jelaga lambat disertai dengan hanya pembentukan CO 2 terjadi di atas 400 °C tetapi tidak selesai dalam kisaran suhu yang dipelajari.
Diketahui bahwa NO x dapat meningkatkan oksidasi jelaga. [ 1 , 15 , 16 , 25 ] Mekanisme oksidasi berbantuan NO x mengacu pada oksidasi katalitik NO menjadi NO 2 selama oksidasi katalitik jelaga, dengan aktivitas oksidasi NO yang tinggi dari katalis dan peningkatan adsorpsi spesies NO x (termasuk NO dan NO 2 ) pada permukaan katalis memainkan peran penting dalam pembakaran jelaga. [ 1 , 11 , 25 ] Penghambatan oksidasi jelaga yang diamati dapat dikaitkan dengan aktivitas oksidasi NO yang rendah serta adsorpsi NO x yang sangat kuat pada permukaan katalis.
Untuk menghilangkan penghambatan NO pada pembakaran jelaga, reduksi katalitik selektif NO (SCR) dengan adanya oksigen dapat diwujudkan dengan menggunakan C 3 H 6 24 atau CO [ 26 , 27 ] sebagai agen pereduksi. Gambar 3b menunjukkan hasil yang diperoleh untuk oksidasi jelaga dengan adanya NO dan CO. Dengan adanya CO dalam campuran reaksi, penghambatan NO pada pembakaran jelaga praktis tidak diamati ( T maks = 477 °C), tanpa CO yang muncul dalam produk di atas 180 °C. Hal ini terkait dengan konversi NO melalui SCR dengan CO menjadi N 2 sebelum oksidasi total CO.
2.3 Sampel Monolit
Untuk mempelajari pembakaran jelaga dalam kondisi yang lebih realistis, komposisi katalitik yang paling menjanjikan diendapkan pada blok kordierit. Untuk penelitian ini, monolit sarang lebah kordierit kecil dengan dimensi 7 × 7 × 15 mm dan ukuran sel sarang lebah 1,5 mm digunakan (Gambar 4a,b ). Komposisi Ag/1Ce1Mn didukung pada monolit sarang lebah kordierit menggunakan impregnasi dengan suspensi Ag/1Ce1Mn serta impregnasi dengan larutan berair Mn(NO3 ) 2 dan Ce(NO3 ) 3 atau teknik sol-gel sitrat untuk mengendapkan komposisi oksida 1Ce1Mn diikuti oleh impregnasi blok yang dimodifikasi oksida dengan larutan [Ag(NH3 ) 2 ] NO3 untuk pengendapan Ag berikutnya (untuk rincian lihat SI).

Gambar 4
Buka di penampil gambar
Presentasi PowerPoint
(a,b) Gambaran umum monolit yang digunakan dan (c–f) sampel Ag/1Ce1Mn/monolit yang disiapkan dengan teknik sol-gel: (a) tampilan umum monolit dan (b) gambar SEM sel sarang lebahnya; (c) SEM dan (d) EDS multilapis. (c) Gambar lapisan oksida 1Ce1Mn pada permukaan monolit, (e) Gambar SEM, dan (f) STEM komposit Ag/1Ce1Mn dalam sampel Ag/1Ce1Mn/monolit.
Hasil spektroskopi Raman dan studi SEM dari sampel monolit menunjukkan bahwa impregnasi monolit kordierit dengan suspensi Ag/1Ce1Mn, meskipun komposisi dan mikrostruktur komposit dipertahankan, tidak memungkinkan pembentukan lapisan katalitik kontinu pada permukaan monolit (Gambar. S7a, S8 ). Pengendapan komposisi oksida 1Ce1Mn dengan impregnasi dengan larutan garam berair mengarah pada pembentukan film oksida kontinu, tetapi pembentukan komposit 1Ce1Mn dengan mikrostruktur nanodomain tidak terjadi (Gambar. S7c, S9 ). Pada saat yang sama, penggunaan teknik sol-gel untuk pengendapan komposit oksida 1Ce1Mn memungkinkan tercapainya komposisi, mikrostruktur, dan distribusi oksida yang relatif seragam pada permukaan monolit (Gambar. S7b , 4c ). Penambahan 10 wt.% bubuk 1Ce1Mn dalam sol lebih meningkatkan distribusi komposit di atas permukaan monolit karena penurunan penyusutan xerogel di bawah kalsinasi (sampel dilambangkan sebagai Ag/1Ce1Mn*/monolit). Morfologi dan komposisi lapisan Ag/CeMn* awal yang diendapkan pada permukaan kordierit melalui pendekatan ini tetap praktis tidak berubah bahkan setelah penuaan sampel pada 650 °C selama 12 jam dalam kondisi statis (Gambar S10 ).
Aktivitas katalitik sampel Ag/1Ce1Mn/monolit yang disiapkan dengan teknik sol-gel sitrat dipelajari dalam kondisi kontak longgar dalam reaktor aliran tubular dalam mode reaksi terprogram suhu (TPR) dalam aliran 10 vol.% O 2 dalam helium. Jelaga model diaplikasikan ke monolit dari suspensi etanol dengan impregnasi berulang dengan pengeringan antara blok dalam oven konveksi pada suhu 60 °C (untuk detailnya lihat Informasi Pendukung ).
Oksidasi jelaga pada sampel Ag/1Ce1Mn/monolit dalam kondisi kontak longgar dalam aliran 10 vol% O 2 dalam helium berlangsung dalam kisaran 450–670 °C dengan dua laju pembakaran maksimum antara 552 dan 628 °C (Gambar 5a ), yang lebih tinggi daripada katalis bubuk Ag/1Ce1Mn ( T maks = 448 °C) dalam kondisi kontak rapat dalam reaktor aliran (Gambar 5b ). Kehadiran dua puncak pembakaran jelaga pada katalis monolit disebabkan oleh lapisan terputus-putus dari komposit Ag/1Ce1Mn pada permukaan monolit (Gambar 4c,d ): bersama dengan area berpori Ag/1Ce1Mn yang terdistribusi secara seragam pada permukaan monolit, ada area permukaan monolit itu sendiri, yang disebabkan oleh penyusutan lapisan xerogel berpori yang dihasilkan setelah kalsinasi. Akibatnya, sebagian jelaga yang diendapkan pada komposit Ag/1Ce1Mn berpori terbakar pada suhu yang lebih rendah, sedangkan jelaga yang diendapkan pada permukaan monolit terbakar pada suhu yang lebih tinggi. Akan tetapi, pembakaran jelaga pada sampel Ag/1Ce1Mn/monolit dalam kedua kasus hanya disertai dengan pembentukan CO 2 . Sebaliknya, pembakaran nonkatalitik pada monolit murni berlangsung dalam kisaran 500–680 °C dengan laju maksimum pada 645 °C dan disertai dengan pembentukan CO dan CO 2 (Gambar S12 ). Hal ini, serta penurunan suhu pembakaran jelaga hingga 628 °C dibandingkan dengan monolit tanpa katalis, mengonfirmasi partisipasi komposit Ag/1CeMn dalam pembakaran jelaga pada permukaan monolit baik sebagai hasil dari luapan oksigen aktif dari komposit Ag/1Ce1Mn ke permukaan blok atau oksidasi CO yang terbentuk selama pembakaran jelaga nonkatalitik dalam sampel Ag/1Ce1Mn/monolit. Berdasarkan gambar EDS multilayer (Gambar S11 ), keberadaan beberapa Ag pada permukaan monolit yang tidak tertutup dengan komposit Ag/1Ce1Mn juga dapat memengaruhi pembakaran jelaga di atas sampel Ag/1Ce1Mn/monolit di daerah suhu rendah dan tinggi karena kandungan perak yang lebih rendah dalam komposit Ag/1Ce1Mn dan modifikasi permukaan monolit.
Gambar 5
Buka di penampil gambar
Presentasi PowerPoint
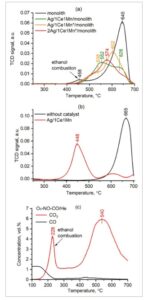
(a) Laju pembakaran jelaga di atas sampel monolit dalam kondisi kontak longgar dan (b) di atas katalis bubuk Ag/1Ce1Mn dalam kondisi kontak rapat dalam reaktor tubular dalam aliran 10 vol.% O 2 dalam helium, (c) Profil konsentrasi CO 2 , dan CO selama oksidasi jelaga di atas sampel Ag/1Ce1Mn*/monolit dalam kondisi kontak longgar dalam reaktor tubular dalam aliran 10 vol.% O 2 , 0,1 vol.% NO, dan 1,25 vol.% CO dalam helium. Ag/1Ce1Mn*/monolit dan 2Ag/1Ce1Mn*/monolit adalah sampel yang diperoleh dengan pendekatan sol-gel dengan penambahan bubuk komposit 1Ce1Mn 10 wt.% dalam sol.
Pengenalan bubuk 1Ce1Mn (10 wt.%) ke dalam sol yang digunakan untuk impregnasi monolit menyebabkan pergeseran profil pembakaran jelaga ke arah daerah suhu rendah untuk sampel Ag/1Ce1Mn*/monolit dengan dua laju pembakaran maksimum pada 530 °C dan 602 °C yang dapat dibedakan (Gambar 5 ). Penurunan yang diamati dalam suhu pembakaran jelaga di daerah suhu tinggi dikaitkan dengan perbaikan dalam struktur lapisan 1Ce1Mn karena penurunan penyusutan xerogel selama perlakuan panas. Peningkatan jumlah perak yang diterapkan menjadi 2 wt.% memungkinkan pengurangan suhu pembakaran jelaga pada sampel 2Ag/CeMn*/monolit di bawah 600 °C (Gambar 5 ).
Oksidasi jelaga dengan adanya NO x ─CO juga dipelajari untuk sampel Ag/1Ce1Mn*/monolit dalam kondisi kontak longgar dalam reaktor aliran tubular. Hasil yang disajikan dalam Gambar 5c menunjukkan bahwa tidak ada penghambatan pembakaran jelaga oleh NO yang diamati ketika CO hadir dalam campuran reaksi sesuai dengan hasil yang diperoleh untuk sampel bubuk Ag/1Ce1Mn (Gambar 3b ). Selain itu, hilangnya CO secara praktis lengkap dalam produk diamati untuk sampel Ag/1Ce1Mn*/monolit pada suhu di atas 250 °C.
Meskipun hasil yang relatif baik diperoleh untuk sampel Ag/1Ce1Mn*/monolit dalam oksidasi jelaga, penggunaan kembali sampel tersebut dalam proses selanjutnya mengakibatkan penurunan bertahap dalam aktivitas oksidasi jelaga (Gambar S11a ). Perlakuan termal berulang hingga 700 °C di bawah aliran gas (40 mL/menit) selama oksidasi jelaga diikuti oleh pendinginan terbukti mengakibatkan delaminasi katalis (Gambar S11b,c ) karena ketidakcocokan koefisien ekspansi termal (CTE) untuk keramik kordierit (CTE ∼2 × 10 −6 K −1 ) dan komposit (CTE ∼11 × 10 −6 K −1 dan α∼9 × 10 −6 K −1 untuk ceria dan MnO x , masing-masing). Oleh karena itu, diperlukan peningkatan ketahanan lebih lanjut dari lapisan katalis pada monolit. Hal ini dapat dicapai dengan menggunakan lapisan antara [ 28 ] atau monolit korundum (CTE ∼8 × 10 −6 K −1 ).
3 Kesimpulan
Katalis serbuk Ag/CeO2 , Ag/MnOx , dan Ag/CeMnOx dengan rasio molar Ce:Mn yang berbeda disiapkan dengan metode sol-gel sitrat dan dipelajari dalam oksidasi jelaga di bawah kondisi model dan mendekati kondisi nyata. Metode sol-gel sitrat telah terbukti memberikan pembentukan komposit CeMnOx dengan mikrostruktur nanodomain karena pencampuran komponen yang seragam selama pembentukan gel dan karena kelarutan MnOx yang terbatas dalam struktur fluorit CeO2 . Pengaruh timbal balik oksida cerium dan mangan dalam katalis Ag/CeMnOx termasuk peran rasio Ce/Mn dalam pembentukan mikrostruktur nanodomain komposit CeMnOx dan juga peran spesies Ag yang terdistribusi pada permukaan komposit dirinci. Kehadiran gabungan nanodomain CeO2 dan MnOx yang didistribusikan secara acak dalam komposit CeMnOx dengan rasio molar Ce:Mn sebesar 1:1 mencegah sintering nanopartikel CeO2 yang memastikan aktivitas dan stabilitas tinggi komposit Ag/1Ce1Mn yang berbeda dengan sampel Ag/Ce dan Ag/3Ce1Mn yang dinonaktifkan setelah penuaan. Kehadiran NO dalam campuran reaksi menghambat proses oksidasi jelaga karena oksidasi kompetitif jelaga dan NO. Penambahan CO ke dalam campuran reaksi NO + O2 berkontribusi pada implementasi efektif proses gabungan oksidasi jelaga dan SCR NO menjadi N2 oleh CO.
Katalis Ag/1Ce1Mn/monolitik telah berhasil disiapkan menggunakan teknik sol-gel sitrat untuk mengendapkan komposit CeMnO x di atas kordierit. Metode tersebut memungkinkan pembentukan lapisan kontinu komposit CeMnO x dengan mikrostruktur nanodomain di ruang berpori monolit. Telah ditetapkan bahwa penggunaan bubuk Ag/1Ce1Mn dan katalis Ag/1Ce1Mn/monolitik meningkatkan oksidasi selektif jelaga menjadi CO 2 di bawah 500 dan 600 °C, masing-masing.

