
Abstrak Grafis
Suatu zat antara Wheland yang stabil secara kinetik dari substitusi aromatik elektrofilik pada ferosena diisolasi dari reaksi ion diferrocenylphosphenium dengan alena 2-(trimetilsilil)-2,3-pentadiena dan dikarakterisasi sepenuhnya.
Abstrak
Reaksi ion diferrocenylphosphenium dengan empat alena terminal mengikuti dua jalur yang berbeda, melalui karbokation alil atau vinil, yang berlanjut dengan reaksi substitusi elektrofilik pada satu gugus ferrocenyl untuk membentuk zat antara Wheland yang persisten dan akhirnya garam alkenildiferrocenylphosphonium. Reaksi ion diferrocenylphosphenium dengan 2-(trimetilsilil)-2,3-pentadiena menghasilkan zat antara Wheland yang stabil dari ferrosena dalam hasil yang tinggi, yang diisolasi dan dikarakterisasi sepenuhnya.
1 Pendahuluan
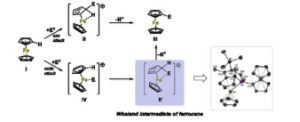
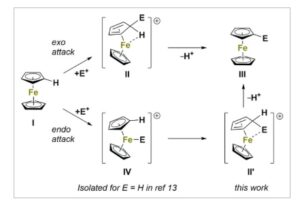
Ion arenium, sering disebut sebagai zat antara Wheland, [ 1 ] adalah kompleks σ sementara yang umumnya terjadi pada reaksi substitusi aromatik elektrofilik (S E Ar). [ 2 ] Meskipun isolasi zat antara ini secara umum dianggap menantang karena masa hidupnya yang pendek, sejumlah contoh yang sepenuhnya dikarakterisasi telah dilaporkan dalam literatur, dengan yang paling sederhana adalah ion benzenium [C 6 H 7 ] + yang diperoleh dengan protonasi benzena. [ 3 – 10 ] Untuk S E Ar pada ferosena, dua mekanisme yang mungkin dibahas ( Skema 1 ): serangan ekso elektrofil pada cincin siklopentadienil (Cp) yang mengarah pada pembentukan kompleks σ endosiklis II , atau serangan endo elektrofil pada atom besi IV , diikuti oleh penataan ulang menjadi kompleks σ II’ . [ 11 , 12 ] Eliminasi proton dari II atau II′ menghasilkan produk substitusi akhir III . Dalam dekade terakhir, Malischewski dan Meyer melaporkan protonasi ferrosena menghasilkan [Cp 2 FeH] + , yang dapat dianggap sebagai contoh untuk reaksi perantara IV . [ 13 ] Sejauh pengetahuan kami, perantara ferrosena Wheland ( II atau II′ ) sejauh ini belum pernah diisolasi.
Skema 1
Buka di penampil gambar
Kekuatan Gambar
Mekanisme S E Ar pada ferrosena. [ 11 , 12 ] Diadaptasi dari Malischewski dan Meyer et al. [ 13 ]
Alena adalah diena kumulatif yang menunjukkan karakteristik dan reaktivitas unik karena susunan strukturalnya. [ 14 , 15 ] Contoh utama aktivasi alena oleh senyawa golongan utama, asam Lewis kuat berbasis borana sebelumnya digunakan sebagai katalis dalam reaksi siklisasi dengan berbagai alena, atau sebagai reagen dalam reaksi stoikiometri, menghasilkan borana kompleks yang berfungsi sebagai substrat untuk reaksi penggandengan berikutnya. [ 16 ] Terinspirasi oleh karya ini, kami tertarik pada aktivasi alena oleh ion diferrocenylphosphenium [Fc 2 P] + , analog karbena kationik dan asam super Lewis. [ 17 , 18 ]
HOMO yang lebih tinggi pada alena, dibandingkan dengan alkuna, membuatnya rentan bereaksi dengan elektrofil ringan. Tidak seperti asam Lewis berbasis borana, [Fc 2 P] + memiliki pasangan elektron bebas tambahan, yang menghasilkan sifat ambifilik yang berpotensi digunakan dalam serangkaian reaksi yang kontras. Dengan demikian, diharapkan bahwa reaksi kation [Fc 2 P] + dengan substrat kaya elektron pada awalnya akan mengarah pada pembentukan karbokation, yang dapat distabilkan secara intramolekuler, misalnya, melalui interaksi dengan atom besi, atau mengalami reaksi lebih lanjut seperti penataan ulang.
Reaksi ion diferrocenylphosphenium, [Fc 2 P][B(C 6 F 5 ) 4 ], [ 18 ] dengan 3-metil-1,2-butadiena ( s1 ) ( Skema 2 ) pada suhu kamar dipantau oleh spektroskopi NMR 31 P (Gambar S75, Informasi Pendukung). Setelah beberapa menit, sinyal bahan awal pada δ = 183,5 ppm menghilang dan singlet baru pada δ = −80,2 ppm muncul, yang ditugaskan ke perantara Wheland (misalnya, B dalam mekanisme yang diusulkan, vide infra). Selama beberapa menit, zat antara Wheland yang diusulkan bereaksi lebih lanjut untuk menghasilkan ion alkenildiferrokenilfosfonium 1 , sehingga menghasilkan doublet yang berpusat pada δ = −1,6 ppm dengan kopling 1 J ( 1 H– 31 P) pada 489 Hz. Ketika reaksi diulang pada skala preparatif, 1 dapat diisolasi sebagai kristal kuning dengan hasil 72%.
Skema 2
Buka di penampil gambar
Kekuatan Gambar
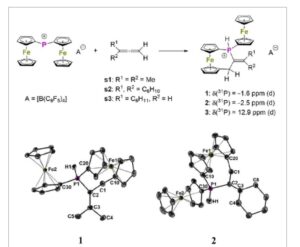
Atas: Reaksi ion diferrocenylphosphenium dengan 3-methyl-1,2-butadiene ( s1 ), vinylidenecyclohexane ( s2 ), dan cyclohexilallene ( s3 ). Bawah: Struktur molekul garam alkenylphosphonium 1 dan 2 setelah HAR. [ 19 – 21 ] Hanya atom H1 yang dimurnikan secara bebas dan anisotropik yang diperlihatkan, sementara semua atom hidrogen lainnya, meskipun juga dimurnikan secara bebas dan anisotropik, serta anion [B(C 6 F 5 ) 4 ] − , dihilangkan demi kejelasan.
Demikian pula, reaksi ion diferrocenylphosphenium, [Fc2P ] [ B (C6F5 ) 4 ] , dengan alena terminal lainnya, yaitu, vinylidenecyclohexane ( s2 ) dan cyclohexilallene ( s3 ), menunjukkan sinyal NMR 31 P awal pada δ = −81,5 ppm yang ditetapkan pada zat antara Wheland, yang dengan cepat berubah menjadi garam alkenylphosphonium yang sesuai 2 dan 3 yang diisolasi pada skala preparatif dalam hasil 44% dan 55%, masing-masing (Skema 2 ). Spektrum NMR 31 P dari 2 mengungkapkan doublet yang berpusat pada δ = −2,5 ppm dengan kopling 1 J ( 1H – 31P ) sebesar 489 Hz. Reaksi alena asimetris s3 menghasilkan campuran stereoisomer. Spektrum NMR 31 P dari campuran reaksi mentah mengungkap dua doublet dalam rasio integral 93:7 pada δ = 13,0 ppm dan δ = −2,6 ppm dengan kopling 1 J ( 1 H– 31 P) masing-masing 488 dan 490 Hz, yang ditetapkan pada isomer Z dan E dari 3 . Upaya untuk memisahkan isomer ini dengan kristalisasi fraksional gagal. Struktur molekul 1 dan 2 konsisten dengan konektivitas molekul yang diperoleh dari penugasan NMR (Skema 2 ).
Sebaliknya, reaksi ion diferrocenylphosphenium, [Fc 2 P][B(C 6 F 5 ) 4 ], dengan 1-metil-1-(trimetilsilil)alena ( s4 ) menunjukkan dua zat antara yang berumur lebih panjang dengan pergeseran kimia 31 P NMR pada δ = −91,9 dan −101,1 ppm, yang ditetapkan ke zat antara Wheland isomerik (misalnya, E1 dan F1 dalam mekanisme yang diusulkan, vide infra). Zat antara ini sepenuhnya diubah menjadi ion alkenilfosfonium akhir 4 setelah 72 jam ( Skema 3 ). Spektrum 31 P NMR dari 4 menunjukkan doublet dari triplet yang berpusat pada δ = −3,8 ppm dengan kopling 1 J ( 1 H– 31 P) dan 2 J ( 1 H– 31 P) masing-masing 504 dan 17 Hz. Sayangnya, karena stabilitas terbatas dalam larutan, semua upaya untuk mengisolasi 4 tidak berhasil.
Skema 3
Buka di penampil gambar
Kekuatan Gambar
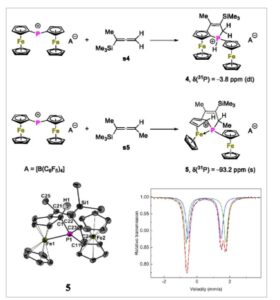
Atas: Reaksi ion diferrocenylphosphenium dengan 1-metil-1-(trimetilsilil)alena ( s4 ). Tengah: Reaksi ion diferrocenylphosphenium dengan 2-(trimetilsilil)-2,3-pentadiena ( s5 ). Bawah, kiri: Struktur molekul dari zat antara Wheland terisolasi 5 , setelah HAR. [ 19 – 21 ] Hanya atom H1 yang dimurnikan secara bebas dan anisotropik yang ditunjukkan, sementara semua atom hidrogen lainnya, meskipun juga dimurnikan secara bebas dan anisotropik, dan anion [B(C 6 F 5 ) 4 ] − dihilangkan demi kejelasan. Bawah, kanan: Spektrum Mößbauer 57 Fe dari 5 , dikumpulkan dalam keadaan padat pada 2 K. Garis hijau dan biru mewakili subspektrum individual, garis merah adalah kurva pemasangan keseluruhan. δ 1 = 0,55 mm s −1 , Δ E Q1 = 2,42 mm s −1 , I rel1 = 52% (hijau); δ 2 = 0,46 mm s −1 , Δ E Q2 = 2,02 mm s −1 , I rel2 = 48% (biru).
Di sisi lain, reaksi ion diferrocenylphosphenium, [Fc 2 P][B(C 6 F 5 ) 4 ], dengan 2-(trimethylsilyl)-2,3-pentadiene ( s5 ), menghasilkan 5 , intermediet Wheland stabil pertama dari ferrosena (Skema 3 ). Dalam spektrum NMR 31 P, 5 menunjukkan singlet pada δ = −93,2 ppm tanpa kopling 1 J ( 1 H– 31 P). Struktur molekuler mengonfirmasi bahwa aromatisitas satu cincin Cp terganggu oleh atom C1 yang terhibridisasi sp 3 (jumlah sudut 649,1°). [ 19 ] Atom H1 yang terikat pada C1 ditemukan selama penyempurnaan atom Hirshfeld (HAR) dari analisis sc-XRD dan dapat disempurnakan dengan bebas. [ 20 – 22 ] Pasangan elektron bebas atom P(1) menyumbangkan kerapatan elektron ke atom Fe(1) seperti yang ditunjukkan oleh panjang ikatan Fe P yang relatif pendek yaitu 2,2319(6) Å. Dibandingkan dengan bahan awal [Fc 2 P][B(C 6 F 5 ) 4 ], yang menunjukkan interaksi intramolekuler Fe → P yang menstabilkan atom fosfor divalen, [ 18 ] pada 5 stabilisasi ini terbalik Fe ← P. Spektrum Mößbauer 57 Fe dari 5 , diukur pada sampel padat mikrokristalin pada suhu 2 K, menunjukkan dua doublet kuadrupol berbeda dengan intensitas relatif serupa yang sesuai dengan dua atom besi nonekuivalen dalam keadaan oksidasi +II (Skema 3 ). Pemecahan kuadrupol Δ E Q1 = 2,42 mm s −1 dan pergeseran isomer δ 1 = 0,55 mm s −1 (hijau) mirip dengan [Fc 2 P][AlCl 4 ] ( δ = 0,53 mm s −1 dan pemecahan kuadrupol Δ E Q = 2,33 mm s −1 pada 60 K) [ 23 ] dan ferosena ( δ = 0,54 mm s −1 , Δ E Q = 2,43 mm s −1 pada 77 K), [ 13 ] yang dapat dikaitkan dengan atom besi dalam ligan ferosenilik monosubstitusi. Di sisi lain, atom besi kedua menunjukkan nilai pemecahan kuadrupol dan pergeseran isomer yang lebih kecil ( δ 2 = 0,46 mm s −1 , Δ E Q2 = 2,02 mm s −1 , biru), yang kami kaitkan dengan perubahan simetri, yaitu, dari perubahan dalam lingkup koordinasi (misalnya, satu η 4 -Cp dan koordinasi atom P). Zat antara Wheland yang stabil 5 merupakan zat antara yang sangat diinginkan dari mekanisme S E Ar yang diusulkan dari ferosena (Skema 1 ). [ 11 – 13 ] Upaya untuk mengubah 5 menjadi ion alkenilfosfonium yang mirip dengan 4 , dengan pemanasan, menghasilkan campuran produk yang tidak terpisahkan (Gambar S69–S74, Informasi Pendukung).
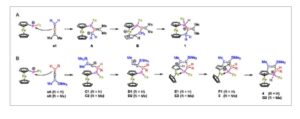
Mengingat produk terisolasi dan zat antara yang diidentifikasi oleh NMR, dua mekanisme berbeda diusulkan untuk menjelaskan pembentukan 1 – 5 ( Skema 4 ). Alena tanpa gugus trimetilsilil (TMS), dicontohkan untuk s1 , menyerang ikatan [Fc 2 P] + dan P C. Pembentukan terjadi pada atom karbon pusat yang terhibridisasi sp (ditandai dengan warna merah), menghasilkan kation alil A (tidak terdeteksi), yang memerlukan rotasi 90° untuk tumpang tindih orbital dan stabilisasi melalui konjugasi. [ 24 , 25 ] Kemudian, kation alil A (ditandai dengan warna biru) mengalami serangan elektrofilik pada cincin Cp kedua dari gugus ferrosenil yang sama untuk menghasilkan zat antara Wheland B (terdeteksi oleh NMR). Langkah tambahan, rotasi 90° juga menjelaskan orientasi karbokation, membawanya lebih dekat ke cincin Cp yang tidak tersubstitusi. Transfer proton dari atom karbon hibridisasi sp 3 dari B ke atom fosfor berlanjut dengan rearomatisasi dan menimbulkan pembentukan ion fosfonium 1 .
Skema 4
Buka di penampil gambar
Kekuatan Gambar
Mekanisme yang diusulkan untuk pembentukan 1 (A), dan 4 dan 5 (B).
Untuk allena s4 dan s5 , yang mengandung gugus TMS, pembentukan ikatan P C terjadi pada atom karbon hibridisasi sp 2 terminal yang paling tidak padat (ditandai dengan warna merah, Skema 4B ) dan menghasilkan kation vinil C1 dan C2 (tidak terdeteksi). Berikutnya, migrasi 1,2-TMS terjadi untuk menghasilkan kation vinil yang lebih terekspos secara sterik D1 dan D2 (tidak terdeteksi), yang kemudian mengalami serangan elektrofilik pada cincin Cp yang sama untuk menghasilkan zat antara Wheland awal E1 dan E2 (terdeteksi). Pergeseran 1,2-proton menghasilkan zat antara Wheland isomerik F1 (terdeteksi) dan 5 (terisolasi), dengan atom karbon hibridisasi sp 3 berikatan dengan fosfor. Pada tingkat teori B3PW91/6-311+G(2df,p) dan pencantuman diklorometana sebagai pelarut, zat antara Wheland 5 yang terisolasi lebih stabil sebesar Δ E = 127 kJ mol -1 daripada zat antara Wheland sementara E2 . Pergeseran proton dari F1 ke atom fosfor kemudian menghasilkan ion fosfonium akhir 4 . Pergeseran proton analog dari 5 ke ion fosfonium G2 yang sulit dipahami tidak teramati. Khususnya, pada tingkat teori yang sama, G2 secara energetik lebih disukai oleh Δ E = 61 kJ mol −1 , yang menunjukkan bahwa 5 distabilkan secara kinetik oleh gugus metil tambahan yang ada di s5 dan tidak ada di s4 .
Kesimpulannya, reaksi ion diferrocenylphosphenium dengan allene terminal (3-methyl-1,2-butadiene ( s1 ), vinylidene-cyclohexane ( s2 ), cyclohexilallene ( s3 ), dan 1-methyl-1-(trimethylsilyl)allene ( s4 )) mengikuti dua jalur berbeda, melalui alil atau karbokation vinil, yang berlanjut dengan reaksi substitusi elektrofilik (S E Ar) pada satu bagian ferrocenyl untuk membentuk zat antara Wheland yang persisten dan akhirnya garam alkenyldiferrocenylphosphonium 1 – 4 . Reaksi ion diferrocenylphosphenium dengan 2-(trimethylsilyl)-2,3-pentadiene ( s5 ) menghasilkan 5 , zat antara Wheland ferrosena pertama yang stabil secara kinetik dan sangat dicari, [ 11 – 13 ] . Selain nilai mendasar dari zat antara Wheland, temuan ini merupakan pintu masuk sintetis ke ferrocenylphosphines yang sangat terfungsionalisasi dan dapat berfungsi untuk memperkuat posisi alena dalam kotak peralatan reagen bagi ahli kimia golongan utama.

